Синтез алкилбензолов на основе хлорпарафинов
В технологии алкилирования бензола олефинами и хлорпарафинами много общего. В качестве катализатора алкилирования бензола хлорпарафинами, как и при алкилировании высшими олефинами, используют каталитические комплексы на основе хлорида алюминия.
Под влиянием хлорида алюминия галогеналкилы поляризуются
![]()
или ионизируются
![]()
Образующиеся карбкатионы (или комплексы с положительным зарядом) атакуют ароматическое ядро, образуя алкилбензолы.
На практике каталитический комплекс для проведения алкилирования бензола хлорпарафинами готовят не только непосредственно из хлорида алюминия, но и из металлического алюминия.
Возможность применения металлического алюминия в качестве катализатора алкилирования бензола известна еще с конца XIX в. Однако работы Крафтса и Радзивановского по использованию металлического алюминия были надолго забыты, и лишь в конце 40-х годов металлический алюминий как катализатор алкилирования снова привлек внимание исследователей. В этот период
Азатян одним из первых вновь использовал металлический алюминий при алкилировании бензола и других ароматических углеводородов алкилхлоридами С1 —С4 [230].
При алкилировании бензола различными галогеналкилами в работах [231 — 233] был использован хлорид алюминия Радзивановского, получаемый взаимодействием металлического алюминия с хлоридом водорода, а при взаимодействии металлического алюминия с алкилхлоридами в среде ароматических углеводородов образуется темно-красный маслянистый нижний слой [234, 235]. Выяснилось [236], что этот продукт представляет собой активный каталитический комплекс, подобный образуемому с алкилароматическими соединениями хлоридом алюминия, такой комплекс можно использовать при алкилировании многократно.
Технологические аспекты применения в производстве высших алкилбензолов через хлорпарафины каталитического комплекса, получаемого на основе металлического алюминия описаны в работе [237].
Процесс образования комплекса протекает по следующему стехиометрическому уравнению:
![]()
Исследование влияния температуры на образование комплекса в избытке алкилароматического углеводорода и хлористого водорода показало, что скорость реакции в диапазоне 20—80 °С изменяется слабо.
Энергия активации брутто-процесса составляет 21—25 кДж/моль. Низкая энергия активации обусловлена влиянием диффузионных ограничений [237].
С повышением температуры приготовления комдлекса усиливается протекание побочных р£акций деструктивного разложения алкилароматических углеводородов, приводящих к образованию низкомолекулярных газообразных продуктов. Поэтому температуру приготовления комплекса ограничивают на уровне 50 °С.
Большое влияние на скорость образования комплекса оказывает строение используемого алкилароматического соединения. По уменьшению реакционной способности алкилбензолы располагаются в ряд: этилбензол > толуол > ксилолы > изопропилбензол > бутилбензол > децилбензол.
При получении высших линейных алкилбензолов, используемых для производства синтетических моющих средств (особенно бытового назначения), важное значение имеет содержание в исходных хлорпарафинах примесей ди- и трихлорпроизводньгх, оказывающих отрицательное влияние на цветность получаемого сульфонола.
Авторы [238], изучив состав продуктов алкилирования бензола хлорпарафинами методами масс-спектрометрии и ИК-спектроскопии, установили, что дихлоралканы при взаимодействии с бензолом вместо ожидаемых дифенилалканов образуют производные индана и тетралина, по следующей схеме:
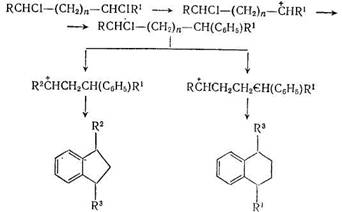
При взаимодействии бензола с трихлоралканами образуются углеводороды общей формулы СnН2n-10:
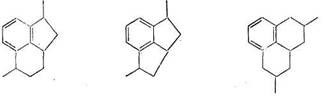
Насыщенные кольца легко окисляются на воздухе при нормальной температуре до гидроперекисей, распад которых приводит к образованию соединений, придающих темный цвет алкилбензолсульфонатам [239].
Образование производных индана и других соединений такого типа возможно и за счет дегидроциклизации алкилбензолов. Выделяющийся при этом водород восстанавливает исходный олефин, обуславливая тем самым образование парафинов. Протекание этой реакции особенно заметно при больших концентрациях хлорида алюминия [240—242].
* Тепловой эффект реакции определен экспериментально.