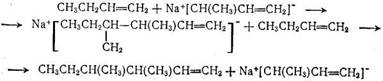Димеризация и содимеризация на щелочнометаллических катализаторах
Реакция димеризации моноолефинов на дисперсиях щелочных металлов впервые описана на основе карбанионного механизма в работе [154]. Этот механизм был распространен на реакции, проводимые в присутствии нанесенных щелочнометаллических катализаторов [150, 151]. В соответствии в этим механизмом, скорость реакции и состав продуктов димеризации зависят только от структуры исходных олефинов, а носителем каталитических свойств является карбанион.
Такой механизм не только не может объяснить некоторые экспериментальные факты, но и противоречит современным представлениям о природе кислотно-основного катализа [146, 148]. Если реакционным центром действительно является карбанион, то при таком механизме роста цепи способность к реакции олигомеризации должны иметь только винильные соединения, обладающие электроноакцепторной способностью, поскольку карбанион является электронодонорным реагентом [155]. а-Олефины, относящиеся к реагентам с электронодонорной способностью [156], не должны присоединять карбанион, и поэтому не должны полимери-зоваться под действием веществ, способных образовывать последние [155].
Как будет показано ниже, экспериментальные данные, полученные при осуществлении реакций димеризации и содимеризации олефинов на щелочнометаллических катализаторах, могут быть достаточно хорошо интерпретированы на основе анионно-координационного механизма, описанного в работах [146, 148]. Этот механизм предусматривает участие в акте роста не кар-баниона, а ионной пары — карбаниона и катиона щелочного металла.
![]() Сравнительное изучение реакций димеризации этилена, пропилена и а-бутилена показало [148, 157], что скорость реакции димеризации этилена и а-бутилена на катализаторе натрий на карбонате калия значительно ниже скорости превращения пропилена.
Сравнительное изучение реакций димеризации этилена, пропилена и а-бутилена показало [148, 157], что скорость реакции димеризации этилена и а-бутилена на катализаторе натрий на карбонате калия значительно ниже скорости превращения пропилена.
Ниже приведены результаты изучения реакции димеризации олефинов на катализаторе натрий на карбонате калия (содержание натрия 3%) [148, 157]:
Этилен | а-Бутилен | Пропилен | |
Температура, С | 150 | 140 | 140 |
Начальное давление, МПа | 13,3 | 11,9 | 10,7 |
Время опыта, ч | 10 | 10 | 20 |
Скорость реакции, г/(г Na-ч) | 0,04 | 0,26 | 2,26 |
Степень превращения олефина,% | 0,66 | 1,35 | 12,9 |
Массовая доля продуктов реакции, % |
|
|
|
бутилены | 72,8 | — | } 0,7 |
пентены |
| — | |
гексены | 27,2 | — | 98,3 |
октены | — | 89,0 | — |
высшие олефины | — | 11,0 | 1,0 |
В результате олигомеризации этилена в основном образуются а-бутилен и З-метил-1-пентен, т. е. преобладают димеризация и тримеризация этилена. Селективность реакции по а-бутилену не очень велика (72,8%), что свидетельствует о том, что в рассматриваемом случае наглядно проявляется первый из сформулиро-ваных выше принципов специфического действия катализаторов димеризации олефинов. Основной продукт реакции — а-бутилен, обладает настолько более высоким сродством к катализатору по сравнению с этиленом, что даже очень низкая степень превращения (0,66%) не обеспечивает избирательности действия катализатора.
Незначительная скорость димеризации этилена связана, по-видимому, с трудностью замещения протона у двойной связи:
![]()
Образовавшееся металлорганическое соединение (I) с винильным карбанионом присоединяет молекулу этилена и превращается в соединение (II) с бутенильным карбанионом:
![]()
Карбанион (II) *, это следует из приведенной ниже классификации карбанионов [145], — очень реакционноспособен и нестабилен:
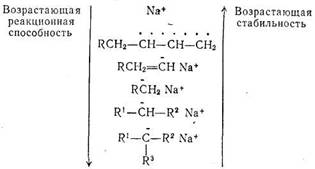
Поэтому указанный карбанион металлирует (а не присоединяет) этилен или его димер с образованием винильного (I) или изобутенильного (III) карбаниона и а-бутилена:
![]()
или
![]()
В пользу этой схемы говорит отсутствие в продуктах реакции 1-гексена — продукта присоединения этилена к нормальному буте-нильному карбаниону (II). Как и следовало ожидать, в основном образуются а-бутилен и З-метил-1-пентен. Последний может быть получен из продукта металлирования а-бутилена — карбаниона (III) и этилена по схеме:
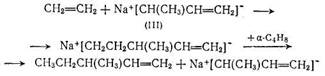
Как показано в работах Мортона [159, 158] и Шатенштейна [160], кислотность а-бутилена, а значит и скорость реакции металлирования этого олефина выше, чем этилена. Этим объясняется и низкая селективность реакции олигомеризации этилена по димеру, и тот факт, что реакция димеризации а-бутилена протекает с более высокой скоростью.
В соответствии с постулируемым анионно-координационным механизмом, при димеризации а-бутилена должен образовываться 3,4-диметил-1-гексен по схеме:
|
Присутствие в реакционной зоне β-бутиленов, которые подаются с сырьем и в небольшом количестве образуются при изомеризации а-бутилена, может привести к образованию натрий-органического соединения с карбанионом (IV):
![]()
Реакция последнего а-бутиленом может дать 5-метил-2-гептен:
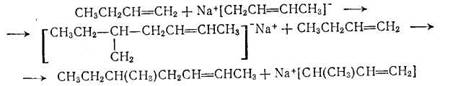
Идентификация продуктов реакции димеризации а-бутилена на катализаторе натрий на карбонате калия на основании результатов хроматографического и ИК-спектроскопического анализа катализата показала, что среди олефинов С8 действительно преобладает 3,4-диметил-1-гексен и в небольшом количестве содержится 5-метил-2-гептен [157]. Хотя степень превращения сырья при димеризации бутиленов была вдвое выше, чем при димериза-ции этилена, селективность по димеру возросла до 89%, что можно объяснить исходя из положения о том, что сродство к катализатору или способность к реакции металлирования у димера а-бутилена намного ниже, чем у димера этилена.
---------------
* Здесь и далее вместо выражения «металлорганическое соединение, содержащее карбанион» будет применяться сокращение «карбанион».