Термическая стабильность активного оксида алюминия
Катализаторы риформинга обычно эксплуатируют при 520—530 °С. Во время регенерации катализатора, кроме высокой температуры, на него воздействует водяной пар, насыщающий кислородсодержащий газ, поступающий в реакционный блок установки риформинга.
При этих условиях длительная работа катализатора требует, чтобы носитель обладал высокой термической стабильностью. Работами [129, 130, 134, 135, 137] показано, что γ-оксид алюминия, полученный в результате прокаливаний мелкокристаллического бемита при 450—600 °С, обладает удельной поверхностью до 200—300 м2/г. Удельная поверхность сохраняется на достаточно высоком уровне вплоть до 800 °С, когда начинается образование новой кристаллической фазы (σ-А12О3). Эта-оксид алюминия, получаемый из байерита прокаливанием при 250—300 °С, имеет поверхность до 300—500 м2/г, она сохраняется на этом уровне до 300—400 °С, затем начинает быстро снижаться [130, 146, 147].
На рис. .2.2 и 2.3 показано изменение удельной поверхности * и кислотности ** оксидов алюминия при прокаливании в токе воздуха в интервале 350—750 °С. Оксид алюминия на основе бемита (А-64) сохраняет практически постоянное значение удельной поверхности (230 м2/г) при прокаливании вплоть до 650 °С, далее она начинает снижаться, но.не резко. Наибольшую удельную поверхность (800 м2/г) имеет образец η-оксида алюминия, полученный на основе почти чистого байерита. Столь высокое значение удельной поверхности по сравнению с литературными данными объясняется как выбором соответствующего режима осаждения, обеспечивающего малые размеры кристаллов, так и частичной конденсацией аргона в очень тонких порах при измерении поверхности адсорбцией этого газа. Поверхность η-оксида алюминия непрерывно падает по мере роста температуры прокаливания и при 650 °С становится несколько ниже, чем удельная поверхность γ-A12O3 при той же температуре. Смесь байерита с бемитом (А-75) образует η-оксид алюминия с поверхностью 500 м2/г, эта величина достаточно стабильна в интер- вале 350—450 °С. Далее поверхность падает так же, как у чистого η-оксида алюминия, но при 750 °С сохраняется на более высоком уровне. Таким образом, наибольшей термической стабильностью обладает γ-A12O3 (А-64).
Изучалось изменение с температурой прокаливания общего числа кислых центров в тех же образцах оксида алюминия (рис. 2.3). Этот показатель определяли по количеству аммиака, адсорбированного оксидом алюминия и удержанного им после десорбции при 175 °С. Для всех образцов число кислых центров возрастает по мере повышения температуры прокаливания, стабильно при 450—550 °С и затем падает. Следовательно, до 450—500 °С идет образование новых центров за счет дегидратации поверхности, а выше 550 °С центры, взаимодействующие с аммиаком, постепенно исчезают. В области стабильных величин кислотность η-А12О3 на 20—30 % выше, чем у γ-А12О3. Сопоставляя данные рис. 2.2 и 2.3, можно заключить, что оптимальная температура прокаливания, обеспечивающая максимальную кислотность с сохранением достаточно высокой удельной поверхности, лежит в интервале 450—550 °С. Результаты получены при проведении прокаливания в токе воздуха, имеющего точку росы около 20 °С. Повышение влажности воздуха, в среде которого осуществляют прокаливание, приводит к значительному снижению удельной поверхности и прочности всех модификаций активного оксида алюминия (рис. 2.3). При прокаливании во влажном воздухе при 550 °С исчезает различие в значениях удельной поверхности двух типов оксида алюминия.
* По методам [133, 138].
** По методу [132]:
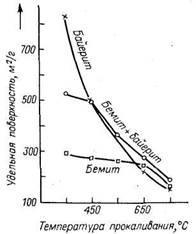
Рис. 2.2. Изменение удельной поверхности оксида алюминия при прокаливании в сухом воздухе гидроксида различного фазового состава.
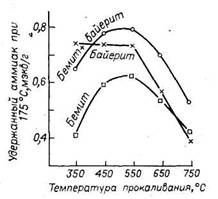
Рис. 2.3. Кислотность образцов оксида алюминия, прокаленных при различной температуре.