Кинетика дегидрирования шестичленных нафтенов
Кинетику дегидрирования шестичленных нафтенов на платиновых катализаторах изучали преимущественно при температурах и давлениях, значительно отличающихся от принятых в процессе каталитического риформинга. За исключением работы [10, 11], данные по кинетике дегидрирования циклогексана и метилциклогексана были получены при температурах, не превышающих 372 °С и давлении от атмосферного до 0,6 МПа [12—16].
Установлено, что при дегидрировании циклогексана и метилциклогексана на монометаллических платиновых катализаторах порядок реакции по углеводороду—нулевой [12—14]. Адсорбционные коэффициенты исходных нафтенов и образующихся ароматических углеводородов одинаковы [12]. Исследование кинетики дегидрирования метилциклогексана на алюмоплатиновом катализаторе (Pt/Al2O3) при 315—372 °С показало, что не только изменение парциального давления углеводорода, но и парциального давления водорода (от 0,11 до 0,41 МПа) не оказывает существенного влияния на скорость реакции [13].
Иные результаты были получены при дегидрировании циклогексана на алюмоплатинорениевых катализаторах (Pt—Re/Al2O3) [15, 16]. Независимо от того, пропускали ли циклогексан над катализатором в смеси с водородом или инертным газом (N2, He, Ar), реакция протекала по первому порядку относительно циклогексана и, следовательно, скорость образования бензола (rБ) выражалась уравнением:
![]()
где k — константа скорости реакции; рцга — парциальное давление циклогексана.
Энергия активации {Е) реакции дегидрирования циклогексана в бензол по данным работы [15] 70,0—72,9 кДж/моль (в зависимости от способа приготовления катализатора), по данным [16] 97,8 кДж/моль. В первой из этих работ данные получены при дегидрировании циклогексана с разбавлением его азотом, во второй — с разбавлением водородом.
В отличие от других исследователей, авторы [10, 11] изучили кинетику дегидрирования циклогексана на алюмоплатиновом катализаторе безградиентным методом при высоких температурах (450 — 500 °С) под давлением от 1 до 7 МПа. следовательно в условиях, близких к применяемымв каталитическом риформинге.
Установлено, что характерная особенность кинетики превращения как циклогексана, так и н-гептана — независимость скорости их превращения от молярного отношения водород : углеводород, если эти реакции проводят в кинетической области на мелком зерне катализатора (до 1 мм). Уравнение скорости общего и отдельных направлений превращения выражается следующим образом
![]()
где ki— наблюдаемая константа скорости i-й реакции; рk — парциальное давление превращающегося углеводорода;
![]() — сумма парциальных давлений углеводородов в реакционной смеси.
— сумма парциальных давлений углеводородов в реакционной смеси.
Из ур. (1.3) следует, что скорость превращения циклогексана на алюмоплатиновых катализаторах пропорциональна концентрационному множителю, тождественному молярной доле реагирующего вещества в смеси углеводородов.
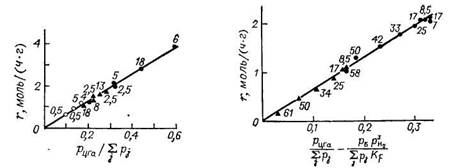
Рис. 1.3. Зависимость скорости образования бензола из циклогексана на катализаторе Pt/Al2O3 (АП-64) от молярной концентрации циклогексана в смеси углеводородов [10, 11 ].
![]()
Рис. 1.4. Зависимость скорости образования бензола из циклогексана на катализаторе Pt/Al2O3

Если скорость дегидрирования циклогексана выразить уравнением лэнгмюровской кинетики
![]()
и предположить, что циклогексан и бензол адсорбируются сильно, их адсорбционные коэффициенты близки по значению [12], а адсорбция водорода мала, то bЦБрЦГа + bБpБ > 1 + bн2Рнги полученная зависимость будет отвечать уравнению (1.3), и может быть представлена также в следующем виде:
![]()
В формулах (1.3)—(1.5) rБ—скорость образования бензола; bн2 bЦГа и bБ— адсорбционные коэффициенты водорода, циклогексана и бензола; рНг, pЦГа и pБ — парциальное давление водорода, циклогексана, бензола; х — молярная доля циклогексана, превращенного в бензол.
Экспериментальными данными, полученными при 470 °С и давлении 1 МПа, подтверждено, что скорость дегидрирования циклогексана на алюмоплатиновом катализаторе является линейной функцией молярной доли циклогексана в смеси с бензолом и что она не зависит от молярного отношения водород : циклогексан (рис. 1.3). Из уравнения (1.5) также следует, что скорость дегидрирования циклогексана не зависит от его парциального давления, что согласуется с наблюдениями, сделанными при изучении кинетики этой реакции на платиновых катализаторах в других условиях [12, 13, 14].
Скорость реакции дегидрирования циклогексана при 470 °С не меняется при повышении парциального давления водорода от 0,8 до 2 МПа, но уменьшается при дальнейшем его увеличении. Подобный результат связан с обратимостью реакции, вследствие чего при 470 °С и парциальных давлениях, превышающих 2 МПа, становятся соизмеримыми скорости прямой и обратной реакций. Применительно к условиям, при которых следует принимать во внимание обратимость реакции дегидрирования циклогексана, скорость ее выражается [10, 11]:
![]()
где ![]() — парциальные давления циклогексана, бензола и водорода;
— парциальные давления циклогексана, бензола и водорода;
![]() — сумма парциальных давлений циклогексана и бензола в реакционной смеси; Кp — константа равновесия.
— сумма парциальных давлений циклогексана и бензола в реакционной смеси; Кp — константа равновесия.
На основе экспериментальных данных эта зависимость выражена графически (рис. 1.4). Наличие подобной зависимости служит указанием на то, что уменьшение скорости дегидрирования циклогексана с повышением парциального давления водорода обусловлено сдвигом равновесия для этой реакции в. сторону циклогексана.
В работе [11] также показано, что в случае осуществления реакции дегидрирования циклогексана на крупном зерне катализатора (3—5 мм) она идет во внутридиффузионной области. В этих условиях скорость дегидрирования циклогексана зависит от молярного отношения водород: углеводород. Однако в современных установках каталитического риформинга преимущественно используют катализаторы с гранулами не более 1,5 мм, а потому диффузионный фактор, связанный с их размером, может оказывать на процесс лишь ограниченное влияние.
Относительные скорости дегидрирования циклогексана и его гомологов в ароматические углеводороды на алюмоплатиновых катализаторах служили предметом немногих исследований [17, 18]. В одной из работ [17] было показано, что при дегидрировании циклогексана, метилциклогексана и этилциклогексана на катализаторе 0,6% Pt/Al2O3 (496 °С, 1,4 МПа) скорости их дегидрирования увеличиваются в ряду: циклогексан < этилциклогексан < метилциклогексан.
Несколько иные зависимости были получены на катализаторе 1% Pt/Al2O3 в других условиях (450 °С, 1 МПа) [18]. Если принять скорость дегидрирования метилциклогексана за 1, то относительные скорости превращения циклогексана и его гомологов равняются:
Циклогексан | 0,9 | 1, 4-Диметилциклогексан | 1,53 |
Метилциклогексан | 1,0 | ||
Этилциклогексан | 1,43 | 1, 3, 5-Триметилциклогексан | 1,24 |
1, 2-Диметилциклогексан | 1,60 | ||
1, 2-Диэтилциклогексан | 1,26 | ||
1, З-Диметилциклогексан | 1,35 | 1, З-Диэтилциклогексан | 1,45 |
1, 4-Диэтилциклогексан | 1,37 |
Таким образом, в сравнении со скоростью дегидрирования циклогексана скорости дегидрирования его гомологов больше. Однако эти различия невелики, в особенности если сопоставить их с соответствующими зависимостями для реакций ароматизации парафинов.