Химическая очистка газов
Преимущество химической очистки состоит в том, что процесс можно направить на удаление специфических загрязнений. Самая известная и самая простая химическая очистка — вымывание аммиака из газов, содержащих диоксид углерода, водой с образованием раствора гидрокарбоната аммония. Эта водная промывка служит одновременно для охлаждения синтез-газа, а чаще всего и является первой ступенью его очистки, особенно, если газ получали среднетемпературной газификацией, так как водой можно отмыть и другие растворимые загрязнения — хлориды, фенолы, жирные кислоты, цианиды.
Способ обессеривания сухой массой, содержащей оксиды железа, ранее весьма распространенный, в настоящее время оказался неэкономичен для установок большой производительности по газу. Это определяется слишком большой потребностью в обслуживающем персонале и в рабочей площади при замене очистной массы, ее переработке и т. д. В настоящее время предпочитают, по крайней мере для грубой очистки, промывку. В этом случае на ступени обессеривания можно применять те же процессы, что и для очистки газов, получаемых из другого сырья, например газификацией тяжелых масел или риформингом бензина кислородом и водяным паром. Для тонкой химической очистки с целью удаления органических сернистых соединений при относительно высокой температуре (≈280°С) можно применять формовку из оксида цинка и из смеси его с оксидом железа.
Большие количества диоксида углерода, например из газа конверсии, удаляют, промывая газ горячим раствором карбоната калия при — 100 С. Различные варианты различаются числом рабочих ступеней и содержанием активаторов в промывном растворе. Активатор оказывает не только каталитическое действие на адсорбционные и десорбционные реакции (и позволяет благодаря этому применять меньшую по размеру аппаратуру), но и защитное антикоррозионное действие. Для тонкой очистки от СО2 можно промывать газ водным раствором аминов или метанированием.
В наши дни химическую очистку всегда осуществляют с циркуляцией и регенерацией промывного раствора. Регенерацию можно проводить в случае очистки от СО2 путем нагревания и отгонки с водяным паром.
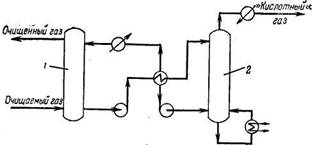
Рис. 89. Схема алкацидного процесса: 1 — абсорбер; 2 — отпарная колонна
При отмывке газов от сероводорода также возможна подобная термическая десорбция (например, в алкацидном процессе). В других процессах отмытый сероводород отделяют, окисляя его кислородом в растворе до свободной серы, выделяя серу фильтрованием (например, в процессах Giammarco — Vetrocoke или Stretford). В случае процессов с термической регенерацией требуется (в зависимости от назначения газа и других обстоятельств) дополнительная тонкая очистка газа от остаточного сероводорода.
Алкацидный процесс применяют для селективного удаления сероводорода или для совместной отмывки сероводорода и диоксида углерода. Используют два различных абсорбента: алкацид ДИК (раствор калиевой соли диэтил- или диметилглицина) —для отмывки от сероводорода — или алкацид М (натриевая соль аланина) — для совместного удаления H2S и СО2. Газ очищают в противоточном абсорбере. Промывной раствор направляют через теплообменник в отпарную колонну, где жидкость нагревается водяным паром, подаваемым противотоком к ней. При этом выделяется так называемый кислотный газ. Очищенную промывную жидкость из отпарной колонны направляют через теплообменник и холодильник снова в абсорбер. Упрощенная схема алкацидного процесса показана на рис. 89 [80].