Низкотемпературная сернокислотная коррозия воздухоподогревателей
Надежность эксплуатации воздухоподогревателей связана с процессами коррозии, развивающимися на поверхности металла, контактирующего с топочными газами. В дымовых газах серосодержащих топлив основными коррозионно-активными компонентами являются оксиды серы (SO2, SО3), кислород, вода.
Процесс низкотемпературной коррозии обусловлен действием серной кислоты, образующейся в результате реакции серного ангидрида (SО3) и водяных паров. При сжигании серы в мазуте первоначально образуется сернистый ангидрид (SO2), при этом около 3 -5% окисляется до SО3 в зависимости от содержания кислорода, влажности и температуры топочного газа [6]. Окисление SО2 до SО3 происходит по реакции:
SO2 + ⅟2O2 ↔ SO3.
Выход SО3 возрастает при увеличении избытка воздуха, По мере его повышения от 5—7 % до значительных величин конверсия возрастает с 3 до 20 % [7].
По современным представлениям, SO3 образуется в результате двух процессов: гомогенного окисления диоксида серы атомарным кислородом в зоне пламени и гетерогенного окисления на твердых поверхностях. Многочисленными исследованиями установлено, что гомогенная реакция SO2 с молекулярным кислородом протекает очень медленно даже при высоких температурах, а реакция S02 с атомарным кислородом протекает довольно быстро и имеет место в зоне пламени вследствие термической диссоциации молекулярного кислорода:
О2 ↔ 2О.
Дополнительное образование атомарного кислорода возможно также при столкновении активированных молекул диоксида углерода, присутствующих в пламени, с молекулой О2:
СО2 + О2 ↔ СО2 +О + О.
Избыточный по отношению к необходимому для полного сгорания топлива кислород реагирует с наиболее окисляемым из образовавшихся продуктов сгорания газов — диоксидом серы. Поэтому сжигание мазута с низкими избытками воздуха приводит к понижению концентрации SО3, однако при наличии подсоса воздуха содержание SО3 значительно возрастает вследствие каталитического окисления диоксида серы.
Fe2O3 катализирует окисление SO2 в SO3. Катализаторами образования SО3 служат сульфат железа (III) на поверхностях нагрева, а также отложения золы, содержащие ванадий и железо, или продукты сгорания, содержащие ванадий.
Образовавшийся серный ангидрид вступает в реакцию с водяными парами дымовых газов с образованием серной кислоты:
SО3 + H2О ↔ H2SO4
При определенной температуре, называемой точкой росы кислоты tp, начинается конденсация H2SO4 на холодных поверхностях нагрева. При этом конденсация происходит при температуре стенки ниже соответствующей точки росы кислоты, которая чаще всего находится в пределах 70—170 С [8].
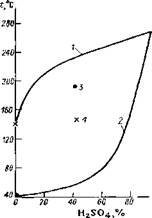
Рис. 7.4. Диаграмма фазового равновесия двухкомнонентной системы H2SO4 — Н2О при РН2O + РSO3 =10 кПа; pН2О = 8,5 кПа [3]
1 — линия росы; 2 — линия кипения; 3 — точка росы при PSО3=0; РН2О = 8,5 кПа; 4 - точка росы при РSO3 = 3Па
Кроме точки росы кислоты процесс коррозии характеризуется также скоростью конденсации кислоты и образованием пленки на поверхности, температурой и концентрацией кислоты.
Температура точки росы в значительной степени зависит от содержания SО3 в дымовых газах, парциального давления образующейся серной кислоты и водяных паров. При этом концентрация SО3 определяется содержанием серы в топливе, избытком воздуха, видом топочной камеры, методом сжигания.
Концентрация H2SO4 в пленке росы обусловливается температурой стенки и давлением паров Н2О и SО3.
На рис. 7.4 показана диаграмма фазового равновесия системы H2SO4 — Н2О для суммарного давления паров PSO3+РН2О = 10 кПа. Нижняя пограничная кривая 2 характеризует зависимость температуры кипения жидкой H2SO4 от ее концентрации, а верхняя кривая 1 — линию росы. Незначительное содержание H2SO4 в паровой фазе резко повышает точку росы по сравнению с точкой росы чистых водяных паров. Охлаждение продуктов сгорания до 150 °С и ниже приводит к пересыщению паров и конденсации кислоты в объеме с образованием тумана [3].
![Зависимость точки росы от содержания серы в мазуте и количества SO3 [9]. На кривых указано количество Sобщ. перешедшее в SO3 Зависимость точки росы от содержания серы в мазуте и количества SO3 [9]. На кривых указано количество Sобщ. перешедшее в SO3](http://www.e-him.ru/img/niz-temp-h2so4-korrozia_clip_image004.jpg)
Рис. 7.5. Зависимость точки росы от содержания серы в мазуте и количества SO3 [9]. На кривых указано количество Sобщ. перешедшее в SO3
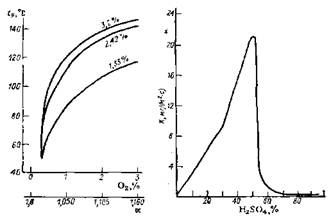
Рис. 7.6 Зависимость точки росы от концентрации свободного кислорода (коэффициента избытка воздуха α) [9]
На кривых указано содержание серы в мазуте
Рис. 7.7. Зависимость скорости коррозии углеродистой стала (0,19 % С) от концентрации серной кислоты [9]
Зависимость точки росы от содержания серы в мазуте представлена на рис. 7. 5. При содержании серы в топливе 1 % точка росы дымовых газов повышается до 130 °С; При содержании серы 1—5 % каждый процент серы повышает tр приблизительно на 4°С. При содержании серы 3—3,5% точка росы дымовых газов составляет прибл. 150—170 °С, значительное снижение наблюдается лишь при содержании серы менее 0,5 %.
Точка росы зависит не только от содержания в топливе серы, серного ангидрида и влажности дымовых газов. Она в значительной степени определяется коэффициентом избытка воздуха α. На рис. 7.6 приведены данные по влиянию коэффициента избытка воздуха на точку росы при сжигании мазутов с содержанием серы 1,3—3,2%. Сжигая мазут с малыми коэффициентами избытка воздуха, можно значительно снизить tp. Так, при содержании кислорода 0,2 % точка росы не зависит от содержания серы в топливе и составляет 52 °С, приближаясь к точке росы чистых водяных паров [9].
Важным фактором в процессе коррозии трубных пучков воздухоподогревателей из углеродистой стали является концентрация H2SO4. Концентрация серной кислоты в пленке росы с понижением температуры стенки понижается. С другой стороны, скорость коррозии металла определяется концентрацией H2SO4. При концентрациях серной кислоты 60—90 % скорость коррозии углеродистой стали сравнительно мала и не зависит от концентрации H2SО4 (рис. 7.7). Максимальная скорость коррозии наблюдается при концентрации серной кислоты примерно 52%, а затем с понижением концентрации коррозия уменьшается.
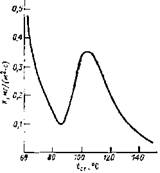
Рис. 7.8. Зависимость скорости коррозии от температуры стенки при сжигании сернистого мазута (2,7— 2,85 % S) [11]
На рис. 7.8 представлена зависимость скорости коррозии металла от температуры стенки при поперечном обтекании. Максимальная скорость коррозии соответствует температуре стенки ниже 70 °С и около 110°С. Минимальное значение наблюдается при температуре стенки не ниже 140 °С и в узком интервале температур 80—90°С.
Таким образом, скорость коррозии металла под действием серной кислоты определяется количеством выпавшей росы, концентрацией H2SO4 в пленке росы и температурой стенки.
Отложения золы играют большую роль в процессе коррозии. Гигроскопичность этих отложений и способность к адсорбции обусловливают поглощение SО3. При остановке печи кислые отложения золы адсорбируют воду, гидролизуются и выделяют кислоту непосредственно на поверхности металла. Это приводит к резкому увеличению скорости коррозии в период остановок.
Использование малосернистого топлива и эксплуатация топочных устройств с минимальным избытком воздуха, поддержание температуры стенки выше точки росы серной кислоты — основные факторы снижения коррозионного разрушения металла.