Высокотемпературная коррозия стали под действием сероводорода
Примеси сероводорода сообщают химическое разрушающее действие рабочим средам в процессах переработки нефти, которые протекают при высоких температурах [1]. Уже при 350 °С содержащиеся в нефти серосодержащие соединения подвергаются термическому расщеплению;
RH + RSH → R — R + H2S (1)
При прочих равных условиях повышение содержания серосодержащих соединений сопровождается (рис. 6.1) увеличением скорости высокотемпературной сернистой коррозии (BTCK). Полнота расщепления увеличивается со временем выдержки при данной температуре, С ростом температуры термический распад охватывает все более сложные и термостойкие сераорганнческие соединения. Например, тиолы при 300°С разлагаются с образованием сульфидов
2(CnH2n+1)SH → (CnH2n+1)2S + H2S (2)
а сульфиды при 400 C — с образованием олефинов
(CnH2n+1)2S → 2CnH2n + H2S (2’)
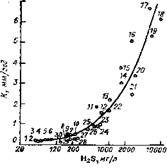
Рис. 6.1. Сопоставление скорости коррозии К углеродистой стали и выделение Н2S из нефтей Урало-Волжской нефтеносной области в условиях перегонки при 350 °С (общее содержание серы, %, указано в скобках): 1 - сураханскан нефть (0,09); 2 —калининская (0,23); 3—мухановская. III пласт (0,28); 4— мурановская, II пласт (0,77); 5—шкаповская. IV пласт (0,59); 5—шкаповская, I пласт (1,67); 7 — дмитровская (1,05); 8 — михайловская, VI пласт (0,61); 9—михайловска, II пласт (0,97); 10—серафимовская, II пласт (0,86j; 11 —серафимовская, IV пласт (0.85); 12—жигулевская (1.52): 13—тарханская (1,99); 14— туймазинская (1,29); 15—мухановская. IV пласт (1,62); 16—мухановская, I пласт(1,10); 17—покровская угленосной свиты (1,15): 18— покровская Башкирского яра (0,56); 19—султановская (1,78); 20—дольненская (1,39); 21—стрельненская (1,66); 22—тархановская угленосная свита (3.10): 23— байтуганская (2,58); 24—яблоневская (2.00); 25 —радаевская (3.05); 26 — серноводская (3,41); 27—староказанковская (2,50); 28—восточно-степановская (2.94); 29— ишимбаевская (3,12); 30 — калиновская (3,60)
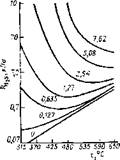
Рис. 6.2. Изокоррозионные кривые для низко-хромистых сталей при различных температурах и парциальных давлениях сероводорода. Цифры на кривых- скорость коррозии, мм/год.
Прямая — граница, отделяющая область возможного протекания ВТСК [2]; парциальное давление H2S; t— температура
Образующийся при распаде по уравнению (1) H2S вызывает ВТСК:
Fe+ H2S → FeS + Н2 (3)
ВТСК развивается с преимущественной диффузией ионов железа через поверхностную пленку в направлении к газообразной (окисляющей) среде. Поэтому наружный слой пленки обогащен не только FeS, но и серой, получающейся за счет частичного окисления
H2S + ½O2 → H20 + S (4)
а также распада FeS2 до более термостабильного FeS и свободной серы:
FeS2 —► FeS + S (5)
Основное влияние на скорость ВТСК и ее характер оказывают рабочие температуры, которые при переходе от одного процесса к другому меняются от 380 °С (печи первичной перегонки) до 430 °С (каталитический риформинг), 550 °С (каталитический крекинг), 625°С (коксование) и 830°С (пиролиз).
Термодинамическая возможность существования более термостабильного FeS (а отсюда сама возможность ВТСК железа сероводородом) определяется температурой и парциальным давлением H2S в газовой фазе (рис. 6.2). Граничная прямая, рассчитанная по данным работы [2], отвечает уравнению:
lg PH2S = 1,34 ∙10-3t — 2,6 (6)
где PH2S—парциальное давление H2S, ат: t — температура газа, С.
ВТСК при высоких температурах может сопровождаться обезуглероживанием карбидов металла, протекающим при высокой температуре:
Fe2C + Н2S —► FeS + СН4 (7)
Такое разрушение [15] протекает главным образом по границам зерен металла (межкристаллитно). Оно может сопровождаться выпадением целых блоков металла.
При температурах ниже 260 С как чистый H2S, так и его газообразные смеси с N2 и H2 при любых парциальных давлениях (т. е. концентрациях) сероводорода практически неагрессивны (хотя термодинамическая возможность коррозии сохраняется). В диапазоне от 200 до 650 °С рост температуры на 100 °С сопровождается увеличением скорости ВТСК в 2—4 раза [3]. Пленки FeS при возрастании температуры превращаются во все более пористые слои, не служащие барьером для проникно- вення сероводорода. Вследствие этого прекращается контроль процесса ВТСК диффузией ионов железа через сульфид и кинетика коррозии начинает определяться скоростью реакции железа с сероводородом.
Низкие, защитные свойства сульфидных пленок связаны с большими внутренними напряжениями из-за высокого (от 2,5 до 4,0) отношения молекулярного объема сульфидной окалины к атомному объему железа (для пленок, способных существенно тормозить коррозию, это отношение составляет 1,8—2,0). Уже при толщине более 0,25 мм сульфидные пленки растрескиваются и отслаиваются [4].