Термодинамические свойства анилина
Термодинамические свойства анилина в состоянии идеального газа приведены в работе [21] Энтальпия образования жидкого анилина равна 31, 1 кДж/моль, стандартная энтропия (в жидком состоянии) составляет 191, 42 Дж/(моль∙К). Теплоемкость при постоянном давлении (C°p энтропия (S°), энтальпия (H°), энтальпия образования из элементов (Hf), изменение функции Гиббса (AG°f) для стандартного состояния, а также логарифм константы равновесия (в единицах давления) для образования 1 моль анилина из элементов для состояния идеального газа и жидкого анилина приведены в табл. 6 [22].
При обобщении данных [20] о термодинамических свойствах анилина в интервале 117—570 °С и 0, 01—20 МПа на основе уравнения состояния Мартина — Хау была построена диаграмма «температура — энтропия», приведенная на рис. 5.
Вязкость анилина при 20 °С составляет 4, 4 мПа∙с и изменяется с температурой:
°С | —5 | 0 | 20 | 40 | 60 | 100 | 120 |
мПа • c | 13, 4 | 10, 2 | 4, 4 | 2, 4 | 1, 6 | 0, 8 | 0, 66 |
Коэффициент теплопроводности жидкого анилина в интервале 0—20°С равен 1, 717∙10-3 Дж/(см∙с∙К), а в интервале 40—80°С он составляет 1, 675∙10-3 Дж/(см∙с∙К) [23].
Коэффициент диффузии паров анилина в воздухе при 20 °С равен 0, 061 см2/с и меняется с температурой так:
°С | 20 | 25 | 30 | 40 | 60 |
d, cm2/c | 6, 1 | 7, 2 | 7, 4 | 7, 9 | 9, 0 |
В водном растворе при 20°С и бесконечном разбавлении коэффициент диффузии равен 9, 2∙10-6 см2/с [23].
Поверхностное натяжение анилина при 10 °С равно 4, 4. 10-2 Н/м, при 20 °С 4, 3∙10-2 Н/м, при 50 °С 3, 85∙10-2 Н/м [25]. Поверхностное натяжение воды на границе с анилином при 30 °С равно 6∙10-3 Н/м, а для ртути на границе с анилином при 20 °С оно составляет 0, 341 Н/м. Криоскопичеcкая константа для анилина 5,87, эбулиоскопическая константа 3, 69 [16].
Таблица 6. Термодинамические свойства анилина
T, к | Cp кДж/(моль∙К) | S°, ДжДмоль. К) | - (G° -H298) T кДж/(моль∙К) | (H°-H298), кДж/моль | H°f кДж/моль | Gf кДж/моль | -lg Kð |
Для состояния идеального газа | |||||||
298 | 108, 48 | 319, 37 | 319, 37 | 0, 00 | 86, 92 | 166, 80 | 29, 205 |
300 | 109, 15 | 320, 08 | 319, 41 | 0, 21 | 86, 79 | 167, 30 | 29, 109 |
400 | 143, 05 | 356, 25 | 324, 10 | 12, 90 | 81, 64 | 194, 98 | 25, 444 |
500 | 170, 86 | 391, 26 | 334, 06 | 28, 64 | 77, 67 | 223, 78 | 23, 363 |
600 | 192, 27 | 424, 46 | 346, 37 | 46, 85 | 74, 65 | 253, 30 | 22, 035 |
700 | 210, 68 | 455, 57 | 359, 77 | 67, 07 | 72, 43 | 283, 28 | 21, 123 |
800 | 225, 21 | 484, 66 | 373, 59 | 88, 89 | 70, 80 | 313, 47 | 20, 454 |
900 | 237, 43 | 511, 92 | 387, 45 | 112, 04 | 69, 67 | 343, 90 | 19, 946 |
1000 | 247, 77 | 537, 50 | 401, 22 | 136, 32 | 69, 12 | 374, 43 | 19, 545 |
Для состояния жидкости | |||||||
298 | — | 191, 42 | — | — | 31, 11 | 149, 18 | 26, 113 |
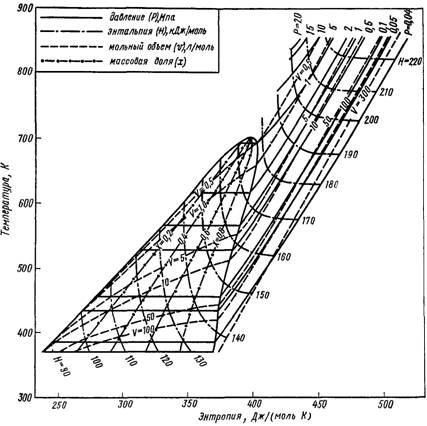
Рис. 5. Диаграмма «температура—энтропия» для анилина.
Дипольный момент анилина при 25 °С равен 1, 56; диэлектрическая постоянная равна 7, 06 при 20 °С и 6, 99 при 25 °С.
Потенциальный барьер внутреннего вращения для связи C—N в молекуле анилина, определенный по термохимическим данным, составляет 14, 36 кДж; весьма близко к этому значение, полученное по спектроскопическим данным (14, 82 кДж). Энергия диссоциации связи C—N равна 381 кДж/моль [26]. Электронный спектр анилина в водном растворе имеет А, макс = 230нм (lge=3, 93) и Aмакс=280нм (lge=3,16) [27]. ИК-спектр анилина приведен на рис. 6, а ПМР-спектр — на рис. 7, где хорошо видны интенсивный сигнал неразличимых протонов аминогруппы (при 3, 6 м. д.) и сигналы протонов бензольного кольца (при 6, 5—7, 5 м. д.). Спектр снят при частоте 60 МГц и температуре 24 °С; растворитель — четыреххлористый углерод. Эталоном является тетраметилсилан (0 |м. д.).
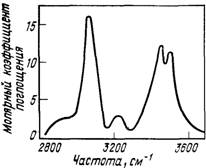
Рис. 6. ИК-спектр раствора анилина в четыреххлористом углероде.
Концентрация анилина 0, 64 М; длина ячейки 1, 58 мм.
При низких температурах анилин в растворах углеводородов дает голубовато-фиолетовую фосфоресценцию, время жизни которой при 77 К равно 4, 7 с. Энергия триплетного состояния анилина 321 кДж/моль. Энергия синглетного состояния, найденная по длинноволновой полосе поглощения, равна 396 кДж/моль. Выход флуоресценции в неполярных растворителях 0, 08, время жизни флуоресценции 3, 9 нс. Потенциал фотоионизации равен 7, 7 эВ [28].
Константы диссоциации при 15, 25 и 40 °С соответственно равны 3, 06∙10-10, 4, 57∙10-10 и 7, 56∙ 10-10.