Гидрокрекинг парафинов на катализаторах риформинга
Гидрокрекинг парафинов, в отличие от гидрогенолиза, — одна из основных реакций каталитического риформинга. В результате гидрокрекинга снижается средняя молекулярная масса парафинов, содержащихся в сырье риформинга, что ведет к повышению октанового числа. Так, при равновесном содержании изомерных парафинов переход от Сn к Cn-1 приводит к повышению октанового числа на 14—15 единиц [17] (см. рис. 1.14). С другой стороны, гидрокрекинг сопровождается газообразованием и, следовательно, снижением выхода жидких продуктов риформинга, а значит и уменьшением селективности процесса. Таким образом, скорости гидрокрекинга должны быть ограничены определенными пределами, которые обеспечивают достаточную эффективность каталитического риформинга.
Гидрокрекинг парафинов на катализаторах риформинга протекает по бифункциональному механизму [54, 83]. Реакция гидрокрекинга н-парафинов включает следующие стадии:
1) дегидрирование н-парафина в н-олефин на металлических центрах катализатора;
2) адсорбция н-олефина на кислотных центрах катализатора с образованием вторичного карбкатиона
![]()
3) превращение вторичного карбкатиона в более стабильный, третичный (это может привести к возникновению углеводорода, изомерного исходному), либо крекинг с образованием меньшего иона карбонил и олефина
![]()
(крекинг проходит предпочтительно по β-связи по отношению к углеродному атому, несущему положительный заряд);
4) изомеризация н-олефина в изоолефин
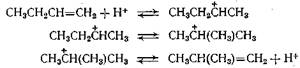
5) гидрирование образовавшихся олефинов (пропилена, бутиленов) на металлических центрах катализатора в соответствующие парафины.
Подтверждением того, что процесс гидрокрекинга на катализаторах риформинга представляет собою бифункциональный катализ, является увеличение его скорости с повышением кислотности катализаторов в результате увеличения содержания галогенов [62, 78]. Поскольку продукты гидрокрекинга — предельные углеводороды, дезактивация катализатора происходит значительно медленнее, чем при каталитическом крекинге.
В соответствии с изложенным выше механизмом реакции гидрокрекинга парафинов метан и этан могут образовываться лишь в незначительных количествах. На первый взгляд такой механизм реакции находится в противоречии с фактом значительного содержания метана и этана в газообразных продуктах риформинга. К другому выводу можно прийти, если учесть, что протекают также и другие реакции, приводящие к образованию этих углеводородов. Так, определенный вклад вносят реакции гидрогенолиза как парафинов, так и ароматических углеводородов: Хотя реакции гидрогенолиза играют весьма ограниченную роль в каталитическом риформинге, все же они идут, особенно в жестких условиях процесса. В частности, метан и этан образуются при гидрогенолизе (гидродеалкилировании) алкилбензолов. Дегидрирование гем-диалкилзамещенных цикло-гексана, как упоминалось выше, также сопровождается образованием метана.
Скорость гидрокрекинга парафинов зависит от их парциального давления [78, 85], парциального давления водорода [58] и растет с увеличением общего давления [17]. Данные о влиянии строения парафина на скорость его гидрокрекинга противоречивы. Так, при риформинге на алюмоплатиновом катализаторе изомеров гексана было показано, что скорости гидрокрекинга 2-метил- и 3-метилпен-тана превышают скорость гидрокрекинга н-гексана соответственно в 3,1 и 2,7 раза [78]. Однако по данным другой работы [80], скорости гидрокрекинга н-нонана, метилоктанов и диметилгептанов на катализаторе риформинга АП-56 приблизительно одинаковы.
Скорости гидрокрекинга н-парафинов значительно возрастают с увеличением числа атомов углерода в молекуле. Так, в [85] показано, что при гидрокрекинге на катализаторе АП-56 константа скорости реакции пропорциональна числу атомов углерода в молекуле н-парафина в четвертой степени:
![]()
где А — коэффициент пропорциональности; N — число атомов углерода в молекуле углеводорода.
По этим данным скорость гидрокрекинга н-октана в 3,2 раза больше, а н-нонана — в 5,1 раза больше, чем скорость гидрокрекинга н-гексана.
Значения энергий активации для реакций гидрокрекинга парафинов на алюмоплатиновом катализаторе составляют для 2-метил и 3-метилпентана 147,3 кДж/моль [78], для н-гептана 130,6 кДж/моль [61].