Олигомеризации этилена c титансодержащими комплексами
Наиболее изученными каталитическими системами олигомеризации этилена являются титансодержащие комплексы. Базовой системой является комплекс тетрахлорида титана с дихлоридом этилалюминия. Процесс олигомеризации этилена на таком катализаторе протекает при температурах, близких к 0°С в полярных растворителях, — ароматических углеводородах, хлорированных парафинах. При использовании неполярных растворителей образуются высокомолекулярные полимеры. Отдельные компоненты комплекса (тетрахлорид титана и дихлорид этилалюминия) сами по себе в реакции олигомеризации этилена неактивны. Взаимодействие тетрахлорида титана с дихлоридом этилалюминия приводит к переалкилированию титана и образованию сильно поляризованного комплекса [123]:
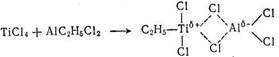
Такой комплекс представляет собой по существу контактную ионную пару, диссоциирующую в высокосольватирующих растворителях на свободные ионы C2H5Ti+Cl2 и АlСl4-.
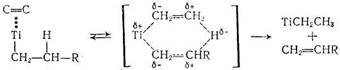
Рассматривая реакцию роста цепи
![]()
как бимолекулярную, а реакцию (β-элиминирования
![]()
как мономолекулярную, легко прийти к выводу, что отношение скоростей роста и вытеснения, определяющее среднюю степень полимеризации, должно зависеть от концентрации мономера. В то же время экспериментальные данные [111, 123] свидетельствуют о том, что молекулярная масса олигомеров этилена, получаемых на титансодержащих катализаторах, не зависит от давления. Отсюда следует, что мономер принимает участие в ограничении цепи. β-Водород переносится по бимолекулярной реакции взаимодействия металлалкила с олефином, минуя промежуточное образование гидрида, через шестицентровое переходное состояние [128]:
По мнению авторов [111] передача цепи на мономер происходит путем переноса β-углеродных атомов водорода в виде гидрид-иона к титану, а далее к координированному на атоме титана мономеру, через промежуточное образование комплекса, в состав которого входит металлалкил и этилен [111]:
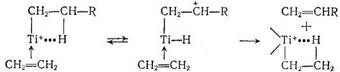
На основании анализа имеющихся данных о влиянии на степень полимеризации состава среды (растворителя) и концентрации катализатора, авторы работы [111] сделали заключение, что рост цепи при олигомеризации идет на ионной паре С2Н5Тi+Сl2—АlСl4-, а ограничение цепи мономера — на катионе RTi+Cl2.
Согласно представленному выше механизму реакции предложена следующая стадийная схема процесса (20 в верхнем индексе означает при 20 °С) [120]:
1) алкилирование TiCl4 дихлоридом этилалюминия с образованием активных центров (X1)
![]()
2) рост цепи путем многократного внедрения этилена по связи Ti—С в активных центрах (RТiCl3АlCl3):
![]()
3) электролитическая диссоциация активных центров на ионы:
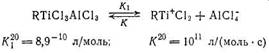
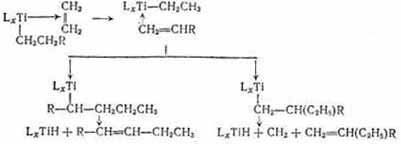
4) передача цепи на мономер:
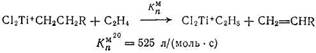
5) дезактивация активных центров:
![]()
Кинетическая модель, разработанная на основании этой схемы, хорошо передает наблюдаемые на практике закономерности протекания процесса.
Как показывает анализ, наиболее существенное изменение свойств продуктов олигомеризации происходит при изменении константы равновесия электролитической диссоциации комплекса RTiCl3AlCl3, зависящей от сольватирующей способности растворителя. Результаты сопоставления теоретических расчетов и экспериментальных данных, полученных при проведении реакции в бензоле, гексане и их смесях, дают хорошее качественное соответствие.
Экспериментальные данные по дифференциальному числовому распределению продуктов реакции характеризуются экспоненциальной зависимостью от степени полимеризации, что характерно для распределения Флори — Шульца.
Доля олефинов С4—С10 существенно возрастает при снижении концентрации катализатора, это свидетельствует об увеличении относительной скорости передачи цепи на мономер.
Одной из интересных особенностей олигомеризации этилена на титансодержащих комплексах является повышение степени полимеризации с ростом температуры, обусловленное тем, что энергия активации реакции роста выше, чем энергия активации переноса β-водорода.
Помимо образования а-олефинов при олигомеризации этилена на титансодержащих комплексах идут побочные реакции образования винилиденовых и внутренних олефинов в результате достройки цепи высшими олефинами, протекающей в результате а) переноса β-водорода растущей цепи на координированный этилен; б) внедрения координированного олефина по связи Ti—С против или в соответствии с правилом Марковникова; в) переноса (β-водорода растущей цепи на металл:
Изомерный состав продуктов олигомеризации этилена под влиянием системы TiCl4—AIC2H5Cl2 определяется температурой, давлением и степенью превращения этилена. Для получения линейных α-олефинов при 20 °С с выходом 90% требуется давление выше 2,0 МПа [119].
Степень превращения этилена рекомендуют выбирать таким образом, чтобы мольное отношение этилен/высшие олефины в жидкой фазе было более 0,8/1. Это предотвращает активное участие высших олефинов в реакции роста и тем самым снижает образование олефинов винилиденовой структуры.
Активность двухкомпонентных систем на основе соединений титана относительно невысока. Скорость реакции составляет 4— 20 моль этилена на 1 г TiCl4/ч. Селективность образования олефинов С6—С20 не превышает 50—60%. Поэтому проводятся интенсивные поиски модификаторов каталитической системы с целью увеличения ее активности и селективности образования линейных α-олефинов.
Достаточно общие соображения свидетельствуют о том, что изменение основности лигандного окружения металла переменной валентности влияет на величину заряда на нем и тем самым на прочность связывания субстрата.
Прочность связи металл—углерод определяет активность катализатора. Ее чрезмерная устойчивость невыгодна для процесса роста цепи. Вводя в состав комплекса электронодонорные добавки, можно понизить заряд на металле и увеличить активность катализатора. Электроноакцепторные лиганды увеличивают относительную частоту реакции β-элиминирования водорода, понижая степень полимеризации.
Комбинируя различные лиганды, можно в принципе очень тонко «настроить» катализатор, подавив, например, возможность координации высших олефинов, и тем самым образование внутренних и винилиденовых олефинов.
Регулирование активности и селективности комплексных катализаторов олигомеризации представляет еще широкое поле для интенсивной исследовательской деятельности.