Механизм ароматизации парафинов, второй вариант
В соответствии с другим механизмом реакции, на металлическом компоненте катализатора риформинга происходит непосредственное превращение парафина в ароматический углеводород [48, 54, 70—72]. Схема превращения н-гексана на платине представлена ниже:
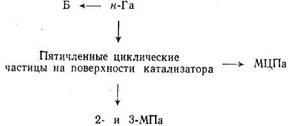
С5- и С6-Дегидроциклизация протекают как параллельные реакции. Платина катализирует также изомеризацию н-гексана в 2- и 3-метилпентаны. В этих условиях парафины, содержащие только пять атомов углерода в цепи, могут изомеризоваться в углеводороды с более длинной цепью. Так, 2-метилпентан может превращаться в н-гексан, который далее реагирует с образованием бензола. Вместе с тем 2-метилпентан может подвергаться дегидроциклизации в метилциклопентан.
Вопрос о вкладе в ароматизацию н-гексана разных путей его превращения в бензол был изучен кинетическим изотопным методом в. условиях импульсного режима при 500 и 550 °С в токе водорода на алюмоплатиновом катализаторе АП-64 [71, 72]. С применением бинарных смесей н-гексан — 1-гексен-14С и н-гексан—метилциклопентан-14С показано, что 34% бензола образуется через гексены, а 18% — через метилциклопентан.
Таблица 1.5. Дегидроциклизация н-гептана на отдельных катализаторах и их смеси [68]
Условия: 482 "С; рн2 1,2 МПа; pГa 0,113 МПа; подача н-Га 16 см3/ч; массовое содержание серы, добавленной к н-Га 0,01%.
Степень превращения н-гептана в углеводород, % | 0,25 г Pt/C | 0,5 г А12О3 | 0,75 г Pt/C+Al2O3 |
Этилциклопентан | — | 0,02 | 0,28 |
1,1 -Диметилциклопентан | — | — | 0,09 |
1,2-Диметилциклопентан | 0,11 | 0,06 | 1,03 |
1,3-Диметилциклопентан | — | 0,07 | 1,04 |
Метилциклогексан | — | — | 0,12 |
Толуол | 0,01 | 0,01 | 0,77 |
Гептены | 0,76 | — | 0,65 |
Циклизации гексана в циклогексан не происходит. Полагают, что 50% бензола образуется в результате непосредственного превращения гексана в бензол, без десорбции промежуточных продуктов реакции. Вместе с тем отмечено, что механизм ароматизации парафинов на катализаторе риформинга АП-64 отличается от механизма на платиновых катализаторах с некислотными носителями заметно большей ролью С5-дегидроциклизации.
Парафины подвергаются также дегидроциклизации на катализаторах риформинга по бифункциональному механизму: дегидрирование на платине, циклизация образовавшихся непредельных углеводородов на кислотных участках носителя. Наглядное подтверждение реальности такого механизма можно найти в работе [68 ]. Из табл. 1.5 видно, что платинированный уголь не катализирует реакцию дегидроциклизации н-гептана, если к последнему добавить 0,01% тиофена (по массе, в пересчете на серу), но сохраняет высокую дегидрирующую способность. Концентрация гептенов не меняется при добавлении тиофена к гептану и близка к равновесной в примененных условиях. Не подвергается дегидроциклизации н-гептан при пропускании над оксидов алюминия. Однако реакция дегидроциклизации протекает, если н-гептан с указанной выше примесью тиофена пропускают над смесью платинированного угля и оксида алюминия. Суммарный выход толуола и алкилциклопентанов составил ≈ 70% от выхода, полученного при дегидроциклизации чистого н-гептана (без примеси тиофена) над платинированным углем.
Поскольку скорость дегидрирования парафинов до олефинов на платине велика, лимитирующей стадией бифункциональной реакции дегидроциклизации должна быть циклизация олефина на кислотных центрах алюмоплатинового катализатора, Поэтому увеличение кислотности алюмоплатинового катализатора, а следовательно, и содержания в нем галогена, должно способствовать увеличению скорости ароматизации парафинов.